Sinoviyal sarkom için yeni tedavi seçeneği otolog T-hücre transfüzyonu Afami-Cel
Sinoviyal sarkom için yeni tedavi seçeneği otolog T-hücre transfüzyonu Afami-Cel
Solid tümörler için çığır açıcı bir çalışmanın sonuçları açıklandı.
İlk sefer savunma hücresi olan Sitotoksik T8 ve T4 hücrelerinin reseptör durumu değişilerek sarkomlu hastaları infüzyon ile verildi ve başarılı sonuç elde edildi.
Sinoviyal sarkom orta yaşlarda görülen nadir tümörlerdendir. Bu hastalığa karşı satandart olarak ifosfamid ve antrasiklin bazlı kemoterapiler kulanılır yanıt oranları ortalam %30 civarındadır. İlk seri kemoterapi sonrası iyi tedavi seçeneği bulunmamaktadır.
Sinoviyal ve myxoid round cell liposarkom tüm sarkomların %5-10 oranını oluşturur ve medyan sağkalım oranı yaklaşık 14,8 aydır.
Sinoviyal sarkom, doksorubisine ve ifosfamid sonrası tedavi seçeneği olmazken, myxoid round cell liposarcoma bu tedavilere ek olarak, erbuline ve trabectedin yanıt elde etmek mümkündür.
Bu tümörler ve tümör mikroçevresi immünoterapi duyarsız grupta yer almaktadır.
Sinoviyal ve myxoid round cell liposarkom MAGE-A4 proteini yüksek oranda ekspre ederler.
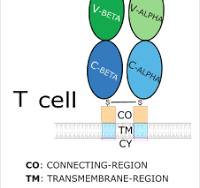
SPEARHEAD-1 çalışması, CD4+ ve CD8+ T hücrelerinin MAGE-A4 resöptörünü tanımaları için vektör aracılığı ile gen modifikasyonu yapıldı. Böylece modifiye edilen CD4+ ve CD8+ T hücreleri Sinoviyal ve myxoid round cell liposarkom hücrelerini kolay tanıyarak immün yanıtın elde edilmesi planlandı.
Kanser mücadelesinde ilk dönüm noktası gen modifikasyonu ile savunma hücrelerin tümör hücrelerini tanıyıp yok edilmesi planlandı.
Sinoviyal ve myxoid round cell liposarkom MAGE-A4 pozitif olan ve aynı zamanda doku antijeni HLA-A*02:01P, -A*02:02P, -A*02:03P, ya da -A*02:06P pozitif olan hastalar için bu tedavi uygun olduğu belirtildi.
İlk aşama hastada lökoferez ile CD4+ ve CD8+ T hücrelerinin toplanması ve bunlara vektör aracılığı ile gen modifikasyonu yapılarak MAGE-A4 proteinine karşı hassaslaştırma reseptör geliştirme aşamasıdır.
İkinci aşama lenfodeplesyon aşaması, hastaya yüksek doz fludarabine ve cyclophosphamide ile yapılmasıdır.
Son aşamada çoğaltılmış afami-cel( CD4+ ve CD8+ ,MAGE-A4 spesifik)periferik damar yolunda hastaya verilerek tedaviye başlanma aşamasıdır.
Bu zor zahmetli aşama sonrası, çoklu tedavi almış ve seçeneği kalmamış hastaların, %37 başarı elde edildi. En sık yan etki Cytokine release sendromu buna bağlı ölüm saptanmadı.
Solid tümörlerde ilk sefer hücre bazlı ve gen değişikliği yapılarak bir tedavi ile başarı sağlandı ve bu tedavi onay otoritelerince çığır açıcı kabul edildi.
Bu çalışma sonrası Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (FDA), Afami-Cel tedavisini daha önce tedavi görmüş Sinoviyal ve myxoid round cell liposarkom hastalarında hızlandırılmış onay ile bir tedavi seçeneği olarak kabul etti.
Kaynak
- Adaptimmune receives U.S. FDA accelerated approval of Tecelra (afamitresgene autoleucel), the first approved engineered cell therapy for a solid tumor. News release. Adaptimmune Therapeutics. August 1, 2024. Accessed August 2, 2024. https://www.adaptimmune.com/investors-and-media/news-center/press-releases/detail/271/adaptimmune-receives-u-s-fda-accelerated-approval-of
- D’Angelo SP, Araujo DM, Abdul Razak AR, et al. Afamitresgene autoleucel for advanced synovial sarcoma and myxoid round cell liposarcoma (SPEARHEAD-1): an international, open-label, phase 2 trial. Lancet. 2024;403(10435):1460-1471. doi:10.1016/S0140-6736(24)00319-2