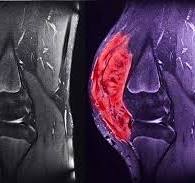
Tenosinoviyal dev hücreli tümör için yeni bir tedavi seçeneği olarak Vimseltinib
Tenosinoviyal dev hücreli tümör için yeni bir tedavi seçeneği olarak Vimseltinib
Tenosinoviyal dev hücreli tümörler orta yaşlarda ve kadınlarda daha sık görülen nadir tümörlerdir.
Genlikle dirsek başta olmak üzere, el ayak eklemleri ve diz eklem yüzeyinde görülür.
Bu tümörler lokal tekrarlarla seyreder. Ana tedavi seçeneği cerrahi olarak tümörün çıkarılmasıdır.
Eklem yüzeylerinde kaynaklanmaları ve sık nüks etme potansiyelleri nedenleri ile cerrahiye bağlı eklem fonksiyon kaybı sık görülür.
Yeni bir tedavi seçeneği ile Tenosinoviyal dev hücre tümörlerin nüks oranlarını azalttığı ve yanıt oranlarını belirgin artırdığı gösterildi.
Tenosinoviyal dev hücre tümörlerinde hastalığın temelinde artmış colony-stimulating faktör 1 (CSF1) gene aktivitesi buna bağlı artmış kontrolsüz CSF1 düzeyidir.
MOTION çalışması oral haftada 2 kez alınan CSFR1 inhibitörü tirozin kinaz inhibitörü olan vimseltinib tedavisinin 24 hafta devam edilmesi durumunda hastalıkta belirgin gerileme olduğu saptandı.
Hastaların %40 hastalığın gerilediği saptandı, aynı zamanda eklem fonksiyonlarındaki iyileşmenin ilaç alanlarda daha iyi olduğu saptandı.
İlaç ilişkili yüzde ödem, alt ekstremitelerde ödem, kaşıntı ve baş ağrısı gibi yan etkiler saptandı. İlaç ilişkili yan etkilere bağlı %6 hasta tedaviyi bırakmak zorunda kaldı.
Bu çalışma sonrası Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (FDA) ilacı ameliyat sonrası tekrarlayan nüks gösteren Tenosinoviyal dev hücreli tümörlerde onaylamak üzere değerlendirmeye aldı.
Kaynaklar
U.S. Food and Drug Administration accepts for priority review Deciphera’s new drug application for vimseltinib for the treatment of patients with tenosynovial giant cell tumor (TGCT). News release. Ono Pharmaceutical, Ltd. August 16, 2024. Accessed August 16, 2024. https://www.ono-pharma.com/en/news/20240816.html
Tap WD, Bhadri V, Stacchiotti S, et al. Efficacy, safety, and patient-reported outcomes of vimseltinib in patients with tenosynovial giant cell tumor: results from the phase 3 MOTION trial. J Clin Oncol. 2024;42(suppl 16):11500. doi:10.1200/JCO.2024.42.16_suppl.11500
European Medicines Agency accepts Deciphera’s marketing authorization application for vimseltinib for treatment of patients with tenosynovial giant cell tumor (TGCT). News release. Ono Pharmaceutical, Ltd. July 19, 2024. Accessed August 16, 2024. https://www.ono-pharma.com/en/news/20240719.html